経皮吸収製剤 ~基礎から応用まで~【第11回】

9.経皮吸収製剤の品質評価 2
前章では国内での品質評価(試験方法)について述べた。本章では海外、特に欧米との品質試験項目の違いにつき述べたい。
9.2 海外での品質規格項目
基本的には、日米欧ともICHで議論されているQ3A~Q3D、Q6Aなどを参考に、各極の薬局方(日本薬局方、米国薬局方(USP)、欧州薬局方(EP))に収載されている局所貼付剤(外用剤)や全身性の経皮吸収製剤として考慮すべき品質規格を考慮して製品特性に応じて設定する。
3極での規格の比較を表8に記載したが、製剤の特性に応じて必要な規格を設定する必要がある。
表8 貼付剤の品質規格項目
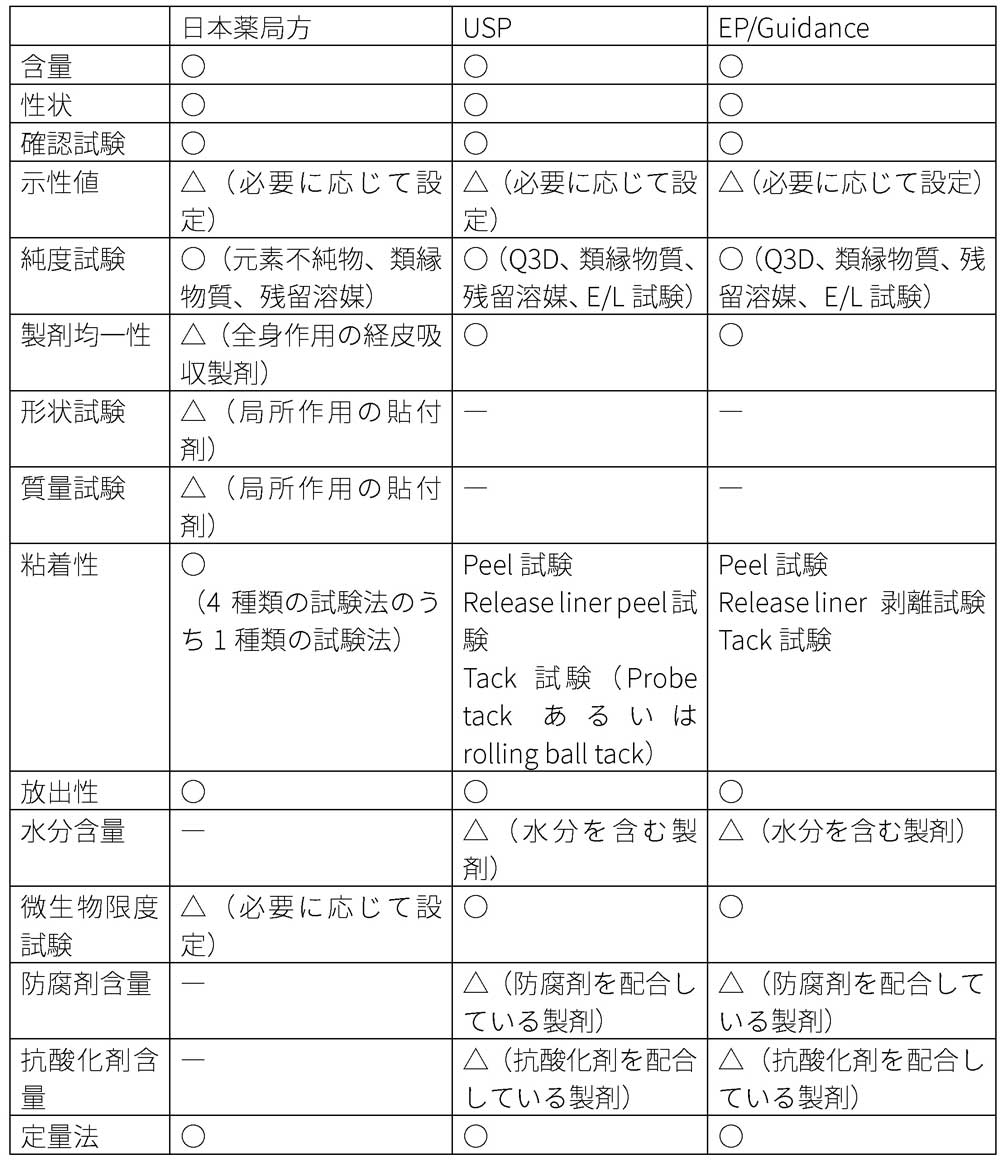
性状(外観)では、主薬の経時的な結晶析出に留意する必要がある。意図的に結晶共存させる製剤もあるが(ホクナリン®テープ、フランドル®テープなど)、品質上問題となるのは経時的に結晶が析出あるいは消失し、それが有効性や安全性、また皮膚への粘着性に影響しないかという点を考える必要がある。海外ではコールドフローと共に照会を受けることが多い。



コメント
/
/
/
コメント