医薬品工場に求められているHSE要件と事例【第65回】

国際化に対応する医薬品会社に必要なHSEとは?
「日本製薬企業に求められる医薬品産業廃棄物の取扱い」
1.製薬企業のあるべき姿
製薬企業の国際化が進む中、企業の多様化を配慮した製薬工場の各種取り組みが求められるようになってきました。日本国内製薬工場は日本の「廃棄物の処理及び清掃に関する法律」:廃掃法に従って廃棄物処理をせねばなりません。又、CSR(企業の社会的責任)、国際法、SDGs、人権尊重の為のGlobal Compact、指導原則などについて世界中のサプライチェーンも含めて、模範を示す事は製薬企業として当然のあるべき姿です。日本の製薬工場から出る廃棄物の種類は医薬品やその原料、原薬が付着した包装資材・プラスチック系包装資材などがあります。これらは医薬品廃棄物としてマニフェストへの記載の分類は汚泥を選択し、焼却が必要です。又、製薬会社の事業所で薬箱の中の期限切れ薬などを廃棄する際は、一般廃棄物扱いはせず、産業廃棄物として扱う事をお勧めします。これらは更に医薬品の場合でも液剤、固形剤と錠剤があり、何れも夫々の曝露リスクや健康への影響リスクの大きいものが多く、取扱いに特別の技術的な注意が必要です。一般的にはこれらリスクを低減する為、感染性廃棄物(特別管理産業廃棄物の一種)として密閉コンテナに入れ、そのまま焼却施設の炉に投入する方法を選ぶことが重要です。病院での取扱いは少し異なりますが、サプライチェーンとしてリスクの低減を図る事を共有されるべきと筆者は考えています。これはお金が関係するため簡単ではありません。一方、欧米のグローバル(国際的)大手企業は廃棄物のGlobal Standardを持っており、これに従って間違っても事故や健康被害が発生することが無きよう運用しています。
<複雑な管理書類>
- 管理票: マニフェストと称して産業廃棄物排出事業者が発行する伝票
- 契約書収集運搬・処分会社への処理委託契約書:産廃処理委託上必須の文書で、社内で共有管理が求められる文書です。
- 付随契約書覚書や合意書、協定書など:原契約書の契約事項を追加・変更する文書です。
- 許可証収集運搬・処分会社から受け取る許可証:無許可業者への委託防止等のリスク対策上、社内の共有管理が必要な文書です。
- 現地確認報告書処分会社等を現地確認した際の報告書:会社情報や過去の実施状況が把握でき、社内での共有が望ましい文書です。
- 事前協議書事前協議の際に行政に提出する届出書:定期的な更新が必要な場合もあり、過去の実施状況の共有が望ましい文書です。
- 行政報告書産業廃棄物処理計画実施状況報告書や交付等状況報告書など:毎年1回作成・提出が必要で、社内で情報共有が望ましい文書です。
<業務の流れ>
産業廃棄物が発生→保管場所を保管基準に従って設置→処理委託先検討→
許可証の確認→委託基準→現地確認、評価→委託先決定→契約書作成 ・WDS/締結→
委託業務開始→マニフェストの運用→文書管理、保管
<契約関係>
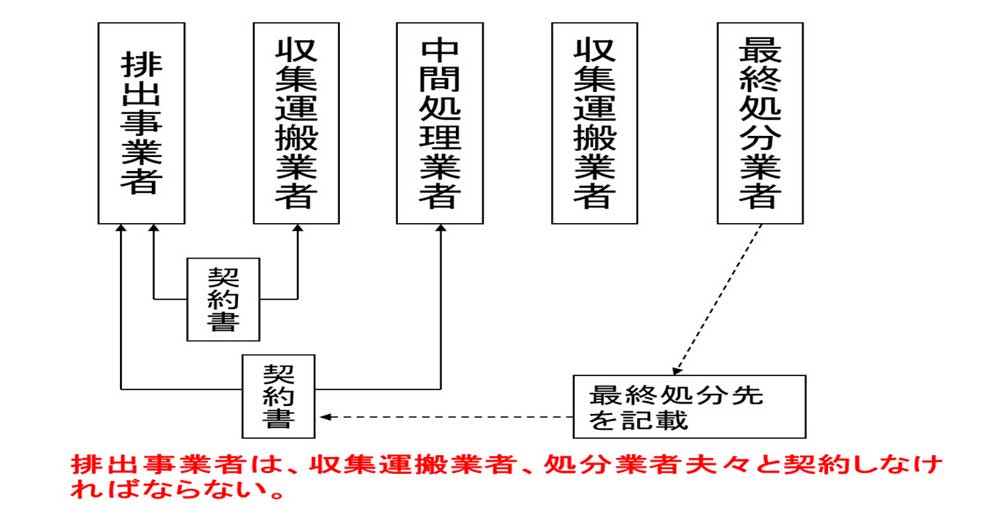



コメント
/
/
/
コメント